Optimización Radioterapéutica mediante el Fraccionamiento de Dosis: Una Perspectiva Radiobiológica sobre la Dinámica del Ciclo Celular
Introducción
La radioterapia constituye uno de los pilares fundamentales en el tratamiento oncológico contemporáneo, con una participación estimada en más del 50% de los protocolos curativos y paliativos a nivel global. Tradicionalmente, la evolución de esta disciplina se ha centrado en el perfeccionamiento de la precisión geométrica —desde la radioterapia conformada 3D hasta la arcoterapia volumétrica modulada (VMAT)— buscando el confinamiento balístico de la dosis en el volumen blanco (Planning Target Volume). Sin embargo, la eficacia clínica de la radiación no depende únicamente de la distribución espacial de los depósitos de energía, sino de una comprensión profunda de la cinética celular y los mecanismos de respuesta biológica.
El desafío central de la física médica y la radiobiología reside en la superación del paradigma de la «dosis única». Si bien la radiación ionizante posee una capacidad letal intrínseca mediante la inducción de rupturas de doble cadena en el ADN (dsDNA), su impacto es discriminatorio. Las células no son entidades estáticas; son sistemas dinámicos que transitan por un ciclo celular compuesto por las fases G_1, S, G_2 y M, cada una con una firma de radiosensibilidad bioquímica específica. Esta variabilidad transforma el tratamiento en un problema de «sincronización temporal»: el tumor es un blanco en constante movimiento biológico.
Bajo esta premisa, el fraccionamiento de la dosis —la fragmentación de la dosis total en fracciones diarias administradas durante varias semanas— surge no sólo como una necesidad logística, sino como una estrategia de manipulación biológica. Este esquema permite explotar la ventana terapéutica, un concepto que define el margen de seguridad entre el control tumoral (TCP) y la toxicidad en tejidos sanos (NTCP). A través del fraccionamiento, el clínico puede inducir una re-sensibilización del tumor mediante la redistribución de las células sobrevivientes hacia fases de vulnerabilidad, mientras garantiza la viabilidad de los tejidos normales a través de la reparación del daño subletal.
Las Bases Radiobiológicas: Las «4 Rs» y la Fase de Redistribución
La respuesta de los tejidos a la irradiación fraccionada está gobernada por las denominadas «4 Rs» de la radiobiología: Reparación del daño subletal, Repoblación, Reoxigenación y, fundamentalmente para este análisis, la Redistribución en el ciclo celular.
Cuando un tumor es irradiado, la población celular no es homogénea en términos de sensibilidad. Como se ha establecido, las células en fase S (Síntesis) presentan una radiorresistencia elevada debido a la disponibilidad de cromátidas hermanas para la recombinación homóloga, mientras que las células en M (Mitosis) y G2 tardía son altamente vulnerables. Una dosis única de radiación produce una «sincronización inducida»: elimina preferencialmente las células en las fases más sensibles (G2/M), dejando una población superviviente enriquecida en células radiorresistentes (fase S).
El Fraccionamiento como Mecanismo de Sincronización Terapéutica
El fraccionamiento permite que, en el intervalo entre sesiones (típicamente 24 horas), las células supervivientes que se encontraban en la fase S (protegidas) progresen a través del ciclo celular y «re-asienten» en las fases G2 y M para la siguiente sesión. Este proceso de redistribución aumenta la eficacia biológica de la dosis acumulada sobre el volumen tumoral.
En contraste, los tejidos sanos de respuesta tardía (como el tejido conectivo o el sistema nervioso) tienen una baja tasa de proliferación. Al fraccionar la dosis, se permite que estos tejidos activen sus mecanismos de reparación del daño subletal sin verse tan afectados por la redistribución, ya que la mayoría de sus células se encuentran en fase G0 (quiescencia), donde la sensibilidad es moderada y la capacidad de reparación es alta.
Modelado Matemático: El Modelo Lineal-Cuadrático (LQ)
La respuesta celular al fraccionamiento se describe mediante el modelo Lineal-Cuadrático, que relaciona la fracción de supervivencia (S) con la dosis (D):
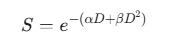
Donde el componente alpha representa el daño letal por un solo impacto (dominante en fases sensibles como M) y el componente beta representa la acumulación de daño subletal (dominante en fases más resistentes como S). La relación $\alpha/\beta$ es un indicador de la sensibilidad de un tejido al fraccionamiento. Los tumores suelen tener valores de alpha/\beta altos (aprox. 10 Gy), lo que indica que son menos sensibles al tamaño de la fracción y más dependientes de la dosis total, mientras que los tejidos sanos tardíos tienen valores bajos (2-3 Gy), siendo muy sensibles a fracciones grandes.
Avances y Tendencias: Del Fraccionamiento Estándar a la Hipof raccionación
La comprensión de la cinética celular ha permitido evolucionar desde el fraccionamiento convencional (1.8 – 2.0 Gy/día) hacia esquemas de Hipof raccionamiento, donde se entregan dosis más altas por fracción en menos sesiones. Esto es particularmente efectivo en tumores con un alpha/\beta bajo (como el cáncer de próstata), donde la biología tumoral se comporta de manera similar a un tejido sano tardío, permitiendo una escalada de dosis con resultados clínicos superiores.
Además, la integración de la Inteligencia Artificial en el monitoreo de la respuesta biológica en tiempo real sugiere un futuro donde el fraccionamiento sea adaptativo. Mediante biomarcadores de imagen funcional, será posible determinar el grado de reoxigenación y redistribución de un tumor específico para ajustar el intervalo entre fracciones de forma personalizada.
Conclusión
La explotación de la radiosensibilidad intrínseca de las fases del ciclo celular mediante el fraccionamiento sigue siendo la piedra angular de la radioterapia clínica. La capacidad de «sincronizar» la entrega de energía con el tránsito de las células hacia fases de vulnerabilidad genómica representa uno de los logros más sofisticados de la física médica y la radiobiología aplicada. El éxito de la terapia no reside solo en la dosis administrada, sino en el respeto riguroso a los tiempos biológicos de reparación y redistribución celular.
Referencias Bibliográficas
- Hall, E. J., & Giaccia, A. J. (2018). Radiobiology for the Radiologist. 8th Edition. Wolters Kluwer.
- Joiner, M. C., & van der Kogel, A. J. (2018). Basic Clinical Radiobiology. 5th Edition. CRC Press. Este texto fundamental establece las bases de las «4 Rs» y el modelo lineal-cuadrático aplicado a la fraccionación clínica.
Pawlik, T. M., & Keyomarsi, K. (2004). «Role of cell cycle in mediating sensitivity to radiotherapy». International Journal of Radiation OncologyBiologyPhysics, 59(4), 928-942. Este artículo revisa exhaustivamente los mecanismos moleculares de los puntos de control del ciclo celular y su